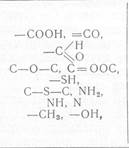К
оглавлению
П.Ф. АНДРЕЕВ
Критерии
генетического различия смолистых веществ нефти
Для геолога, имеющего дело с многоэтажной
нефтеносностью в разрезе изучаемого месторождения, прежде всего интересен
вопрос, имеется ли генетически одна нефть, оказавшаяся в силу своей подвижности
на разных стратиграфических уровнях залегания, или эта нефть разных эпох
образования. Решение этого вопроса важно не столько для непосредственной оценки
данного месторождения, сколько для оценки региональных перспектив нефтеносности
на площади данного бассейна и для поисков новых месторождений.
От геохимического исследования нефтей следует
требовать, чтобы на основе его можно было устанавливать первичные различия в
составе нефтей разного возраста и разных обстановок нефтеобразования, а также
вторичные изменения одной и той же нефти, обусловленные различными внешними
причинами на путях миграции и условиями залегания.
К сожалению, химическая и геохимическая изученность
нефтей и закономерности изменения их состава не позволяют еще отчетливо
дифференцировать первичные и вторичные различия нефтей и решать задачи
генетической корреляции.
Наименее изученной частью нефти является большая
группа веществ, объединяемая обычно одним общим названием асфальтово-смолистых.
Критерием для выделения этой группы являются, пожалуй, только темный цвет,
большой молекулярный вес и некоторые особенности элементарного состава. Попыток
глубокого изучения смолистых веществ до последнего времени было предпринято
совершенно недостаточно. Известны главным образом публикации по разработке
методов довольно грубого разделения и исследования элементарного состава [7,
89, 6].
Вместе с тем становится все более очевидным, что
успешное решение проблемы генезиса смолистых веществ на основе детального
изучения их состава и строения может оказать существенное влияние на скорейшее
решение узловых задач научной теории происхождения нефти.
К настоящему времени в специальной литературе
накопилось достаточно много сведений о химических свойствах отдельных
компонентов нефти, особенно углеводородов, что позволяет сделать попытку
разобраться в процессах образования смолистых веществ и их дальнейших
превращений в условиях существования нефтяных залежей.
После того как будут обсуждены процессы, которые могут
привести к возникновению смолистых веществ, возможно будет представить и
характерные признаки генетически различных групп этих веществ. Последнее может
послужить хорошей основой для постановки экспериментальных работ по
исследованию смолистых веществ нефти, особенно в плане решения важных вопросов
происхождения и изменения нефти в природной обстановке и вопросов формирования
нефтяных залежей.
Вещества смолистой природы образуются в тех или иных
количествах в качестве побочных продуктов при многих химических реакциях из
сравнительно простых исходных веществ. Характерным для этого типа процессов
является увеличение молекулярного веса веществ в результате реакции. Агрегация
исходных молекул в более крупные происходит за счет возникновения новых связей
С-С; С-N-С; С-О-С; С-S-С и может сопровождаться или не сопровождаться
выделением таких простейших соединений, как вода, углекислота, сероводород,
аммиак и т.п.
Развитие этих процессов приводит к возникновению
высокомолекулярных продуктов с их характерными признаками - термопластичностью,
пониженной растворимостью в органических растворителях, аморфностью. С
уменьшением содержания водорода цвет полимеров изменяется в сторону темных
оттенков, растворимость падает, термопластичность уменьшается. В этом же направлении
действует и повышение молекулярного веса полимерной молекулы.
Рассматривая с точки зрения химии высокомолекулярных
соединений смолистые вещества нефти, можно видеть, что последние отличаются от
искусственно приготовленных высокомолекулярных соединений по своим физико-химическим
свойствам. Молекулярный вес смолистых веществ нефти обычно невелик и для
наиболее высокомолекулярной части - асфальтенов - не превышает 1000-1500.
Достоверные сведения о еще более высокомолекулярных веществах нефти - карбенах
и карбоидах -отсутствуют.
Продолжая далее наши сравнения смолистых веществ
нефти, с синтетическими высокомолекулярными соединениями и рассматривая смолы
как естественно образовавшиеся высокомолекулярные соединения, остановим
внимание на некоторых особенностях строения этих двух сходных между собой, но
не идентичных групп веществ.
Синтетические высокомолекулярные соединения по
строению своих молекул делятся на линейные и пространственные. Первые из них
отличаются растворимостью в органических растворителях и термопластичностью, в
то время как пространственные полимеры этими свойствами не обладают.
Среди смолистых веществ нефти имеются соединения,
обладающие свойствами как линейных, так и пространственных полимеров;
силикагелевые смолы растворяются в органических растворителях и размягчаются
при нагревании, в то время как асфальтены этими свойствами обладают не в полной
мере. Имея в виду сравнительно небольшие различия в молекулярных весах
силикагелевых смол и асфальтенов, можно предположить, что первые имеют линейную
структуру молекул, а вторые пространственную.
Синтетические смолы линейной структуры построены из
отдельных повторяющихся звеньев, расположенных в виде двухмерной цепи. В то же
время неплавкие и нерастворимые смолы отличаются тем, что отдельные их звенья
соединены между собой в пространстве так, что вся масса представляет собой
единую макромолекулу.
Синтетические смолы отличаются от естественных тем,
что все молекулы их построены по определенному единому плану, в то время, как
естественные представляют собой сложную систему полимергомологов многочисленных
генетических рядов [1]. Последнее, вообще говоря, характерно для многих
природных органических образований (клетчатка, белки, лигнин и многие другие).
Эти различия основаны на том, что синтетические смолы
получаются обычно при химических превращениях одного вида исходных молекул, в
редких случаях двух или нескольких однородных веществ - мономеров. В то же
время природные смолы имеют своим началом процессы со сложной смесью исходных
веществ, способных к разнообразным превращениям, включающие в себя процессы
образования не только высокомолекулярных, но и низкомолекулярных веществ. В
связи с этим состав природных смол весьма сложен, так как в них сосуществуют
одновременно и продукты полимеризации непредельных соединений и продукты
конденсации гетеро-атомных молекул: вещества, состоящие из линейных и
пространственных молекул. В этой сложной смеси одновременно присутствуют
полимергомологи различных молекулярных весов.
Связи между отдельными фрагментами сложной молекулы в
природных смолах могут осуществляться через различные атомы: С-С; С-О-С; С-S-С; С-N-С, и в силу этого сложные молекулы будут отличаться друг от друга по
своим свойствам даже при одном и том же молекулярном весе и одинаковом типе
строения. Дополнительные усложнения вносит различная степень цикличности и
конденсированности отдельных фрагментов сложной молекулы, имеющая своим началом
различия в строении исходных веществ. Возможность образования смешанных
полимеров - сополимеров, и продуктов конденсационного уплотнения различных
рядов - еще более усложняет строение природных смол.
Образование смолистых веществ в нефти происходит по
тем же самым химическим законам, что и в условиях эксперимента, отличаясь лишь
меньшими скоростями процессов. Энергетическая направленность процессов,
естественно, сохраняется и в природных условиях, особенно если иметь в виду,
что условия нахождения нефти в природе отличаются отсутствием источников
энергии высокого потенциала. В силу последнего обстоятельства все процессы
изменения веществ нефти идут в сторону снижения уровня свободной энергии [3].
Представим систему, состоящую исключительно из
углеводородов метанового, нафтенового и ароматического рядов. Как мы показали
ранее [2], в такой системе обязательно развиваются процессы, приводящие к
образованию, наряду с другими продуктами, смолистых веществ. Естественно
полагать, что образующиеся при этом смолистые вещества по своему элементарному
составу будут отличать полным отсутствием кислорода, серы и азота. Такие смолы получаются
при термической обработке чистых углеводородов.
Образование подобных смол на протяжении коротких
отрезков времени наблюдается не только при высокотемпературном крекинге, но и в
условиях термокатализа А.Ф. Добрянского [4] при относительно низких температурах
порядка 150-200°. Источником смолистых веществ при превращении всех трех
классов углеводородов, являются преимущественно ароматические и частично
нафтеновые углеводороды.
Процессы диспропорционирования водорода приводят к
образованию смолистых веществ из чистых углеводородов в восстановительных
условиях. Эти процессы хорошо известны в условиях лабораторного эксперимента, и
без допущения их наличия нельзя объяснить и многие свойства природных нефтей.
Таким образом, среди смолистых веществ нефтей обязательно должны находиться
смолистые вещества, имеющие в своем составе только лишь углерод и водород. При
этом по мере повышения степени превращенное™ нефти такие смолы будут
характеризоваться все более повышающимися величинами содержания углерода при соответствующем
уменьшении водорода.
К сожалению, мы еще до сих пор не располагаем методами
выделения из состава нефтей смолистых веществ углеводородного характера и
принимаем, что все в целом смолы нефтей представляют собой вещества, имеющие в
своем составе кислород, серу и азот.
Впрочем, Мебери удалось выделить в очень малом
количестве из состава некоторых американских нефтей смолистые вещества состава
С122Н204 и С90H160 [5].
Асфальтены, характеризующиеся своей нерастворимостью в
легком бензине, стоят весьма близко к нейтральным смолам по своему
элементарному составу. Содержание в них гетероэлементов не превышает 10-11%,
составляя в среднем от 2 до 8%. Имеется предположение, что гетероэлементы в
асфальтенах представляют собой одно из звеньев сложных циклов или играют роль
мостиковых связей между отдельными крупными фрагментами сложной молекулы.
Наличие в составе смолистых веществ гетероэлементов
свидетельствует о том, что наряду со смолами углеводородного характера в смеси
с ними присутствуют и смолистые вещества, образовавшиеся иным путем и из других
исходных веществ.
Синтетические смолы, содержащие кислород, серу и азот,
образуются из соответствующих кислородных, сернистых и азотистых соединений в
процессах поликонденсации. Для этих процессов характерно своеобразное
диспропорционирование массы наряду с процессами снижения энергетического уровня
системы. Из молекул некоторых средних размеров возникают, с одной стороны,
более крупные, с другой - более мелкие молекулы.
Можно полагать, что и смолистые вещества нефти,
содержащие кислород, серу и азот, образуются путем поликонденсации спиртов,
кислот, оксикислот, меркаптанов, аминов, альдегидов, кетонов и др.
Соответствующие реакции поликонденсации для этих соединений, приводящие к
образованию высокомолекулярных веществ, хорошо известны в химии
высокомолекулярных соединений [7].
Таким образом, еще одним путем образования смолистых
веществ нефти могут явиться процессы превращения неуглеводородных соединений.
Источником неуглеводородных соединений в
восстановительной обстановке существования нефти могут быть соединения,
характерные для исходных остатков живой клетки.
В то же время в зоне развития окислительных процессов
накопление смол, содержащих атомы кислорода, может происходить в быстром темпе
как за счет углеводородов, так и за счет сернистых и азотистых соединений.
Таким образом, в отношении смол, содержащих
гетероэлементы, задача классификации сводится к установлению источника исходных
соединений.
Среди смол неуглеводородного характера следует
различать смолы относительно невысокого молекулярного веса и
высокомолекулярные. Источником первых следует считать относительно простые
соединения. Высокомолекулярные смолы могли образоваться за счет
низкомолекулярных соединений в результате многократных актов конденсации, что
менее вероятно, или же путем немногих актов конденсации сравнительно крупных
молекул, уже имевших характер смолистых веществ, что больше отвечает
особенностям процессов, происходящих в залежах нефти.
Подавляющее большинство нефтяных залежей, известных к
настоящему времени, существует в обстановке отсутствия окислителей. Вблизи
залежей нефти, как правило, не имеется даже растворенных в воде сульфатов.
В связи с этим следует признать, что окислительные
превращения далеко не характерны для большинства нефтей. Отсюда между прочим
следует, что преимущественным источником образования смолистых веществ,
содержащих кислород, серу и азот, являются имевшиеся в системе реликтовые
соединения, содержащие эти элементы. В целом система нефти в процессе
метаморфизма не накапливает, а расходует ранее имевшиеся запасы
гетероэлементов. Выделение кислорода, серы и азота происходит в виде воды,
углекислоты, сероводорода, аммиака и других простейших соединений.
Часть этих элементов в силу невозможности одноактно
перейти в простейшие соединения сохраняется более или менее длительное время в
системе в виде прочных органических молекул с высокой энергией активации.
Такими молекулами обычно являются сравнительно крупные агрегаты, в частности
молекулы смолистых веществ. Известно, что основная масса кислорода, серы и
азота сосредоточивается именно в смолистых веществах нефти, несмотря на то, что
смолы в составе нефти по сравнению с углеводородами занимают подчиненное
положение [5].
Рассматривая вопрос о порядке выделения гетерогенных элементов
в виде простейших соединений из веществ нефти и о происходящем при этом
изменении элементарного состава смолистых веществ, следует обратить внимание на
прочность отдельных видов связей между атомами. Очевидно, что в первую очередь
будут подвергаться разрыву связи с меньшей энергией диссоциации.
Величина энергии диссоциации связей между атомами
зависит не только от вида этих атомов, но и от типа соединений, в составе
которых находятся интересующие нас связи. Известно из данных [13, 12, 7], что
наименее прочными являются связи углерод-сера в меркаптанах (для пропил-меркаптана
71,4 ккал). Более прочны эти связи в сульфидах и дисульфидах (около 83-85 ккал)
и особенно прочны связи углерод-сера в тиофенах. По соотношениям между
отдельными видами связи углерод-сера, определяемым в составе отдельных нефтей,
можно составить себе представление о стадии ее метаморфизма. В нефтях,
испытавших наибольшие превращения, сера преимущественно будет сосредоточена в
тяжелых смолах и производных тиофена. В средних масляных фракциях серы будет
относительно мало.
Наиболее прочны связи углерод - кислород. Так,
например, для этилового спирта эта величина составляет 90 ккал, для уксусной
кислоты 96 ккал, а для фенола 107 ккал. Вероятно, также прочны связи С-О-С в
соединениях типа фурана, пирана и тому подобных соединениях.
Прочность связей углерод - азот стоит между величинами
диссоциации связей углерод - сера и углерод - кислород, хотя и для азотистых
соединений имеются вещества, у которых энергия диссоциации связей углерод -
азот велика, как, например, производные пиридина и пиррола. Последние наиболее
обычны в составе нефти. Также прочными являются связи углерод- азот в нитрилах
(139 Ккал).
Из этих данных следует, что преимущественно изменениям
при метаморфизме будут подвергаться связи углерод - азот в аминах вместе со
связями углерод - сера в меркаптанах и сульфидах и в последнюю очередь связи
углерод - кислород. В конечном итоге в системе низкокипящих углеводородов
накапливаются производные тиофена и тиофана, пиридина и пиррола.
Для смол, образовавшихся в восстановительных условиях
из гетерогенных соединений захороненных органических остатков будут характерны
связи углерод - сера типа тиофена и тиофана, углерод - азот типа пиридина и
пиррола, углерод - кислород типа пирана, простых эфиров и, ангидридов. Должны
полностью отсутствовать или находиться в сугубо подчиненных количествах связи
типа меркаптанов, аминов жирного и ароматического рядов, спиртов, кислот и
сложных эфиров.
Напротив, в веществах, образовавшихся в окислительной
среде и не испытавших после этого длительных превращений в восстановительной
обстановке, последние связи должны превалировать над первыми. Это следует из
того, что первичными продуктами окислительного воздействия на органические
соединения являются продукты с пониженными значениями энергии диссоциации
связей, так как их образование связана с меньшей затратой энергии. По мере хода
дальнейших превращений эти связи самопроизвольно переходят в другие,
характеризующиеся повышенными значениями величины энергии диссоциации.
Таким образом, на основании различий в характере
связей между атомами гетероэлементов и углеродом можно составить представление
о процессах, приведших к образованию данного типа нефтяных смолистых веществ,
т.е. тем самым решить вопрос об условиях, господствовавших в залежи во время их
образования.
С экспериментальной точки зрения дело сводится к
установлению наличия в веществах смол подвижного водорода, свойственного
меркаптанным, аминным, спиртовым, альдегидным, кетонным, кислотным и другим
функциональным группам.
Смолы окислительного происхождения, не испытавшие
длительного превращения в обстановке отсутствия окислителей, будут содержать
функциональные группы с подвижным водородом, в то время как смолистые вещества,
испытавшие существенные изменения после окисления, будут отличаться отсутствием
групп с подвижным водородом. Чем относительно больше содержится в данной
системе смолистых веществ функциональных групп с подвижным водородом, тем ближе
во времени к моменту исследования проходили в нефти окислительные процессы и
наоборот.
В связи с этим выводом определение подвижного водорода
удобнее заменить определением окислительно-восстановительного потенциала (ОВП),
что, конечно, не исключает необходимости получения интересных данных о
подвижном водороде. В самом деле, всякое органическое соединение, имеющее в
своем составе функциональные группы с подвижным водородом, характеризуется
относительно высокими абсолютными значениями ОВП, отрицательными по знаку. По
мере исчезновения этих функциональных групп величина ОВП все ближе
передвигается к нулю. Измерения ОВП различных каустобиолитов были недавно
проделаны Л.А. Гуляевой и Е.Е. Иткиной [2].
Смолистые вещества, имеющие высокие отрицательные
значения ОВП, в свете этих данных характерны для мало превращенных нефтей или
для нефтей, испытавших в недалеком прошлом интенсивные окислительные
воздействия, и наоборот.
Другим признаком различной генетической природы
смолистых веществ нефти могут явиться различия в величинах их теплот
образования. Известно, что теплота образования соединения, определяемая на
основании измерения величин теплот сгорания, зависит как от элементарного
состава, так и от строения молекул. Возникновение в составе соединения новых
связей с высокими значениями энергии диссоциации приводит к увеличению теплоты
образования, т. е. к увеличению количества энергии, выделяющейся при
образовании данного соединения. Это отражается на величине теплоты сгорания -
происходит уменьшение этой величины.
В процессе метаморфизма в остаточном веществе происходят
исчезновение связей с относительно малой величиной энергии диссоциации и замена
их связями с большей величиной. В пределе система стремится к состоянию
графита, для которого величина энергии диссоциации связи С-С равна 171,7 ккал.
Выделяющиеся при этом из системы соединения, как, например, углекислота, вода и
другие, также характеризуются большими величинами энергии диссоциации связей.
В силу этого, наблюдая изменение величины теплот
образования смолистых веществ или их отдельных составных частей на основании
экспериментально измеримых величин теплот сгорания, можно составить
представление об энергетическом уровне, на котором находится изучаемая система.
С повышением степени метаморфизма величины теплот
образования смол уменьшаются. В начальных стадиях процесса, когда в системе
имеются соединения, образовавшиеся в окислительной обстановке, теплоты
образования велики, а теплоты сгорания малы. По мере исчезновения центров
окисленное™ и потери гетероатомов связи с большой энергией диссоциации заменяются
связями с меньшей энергией.
Теплота сгорания смол увеличивается по мере изменения
элементарного состава и строения в обстановке отсутствия окислителей. Кривая
возрастания величин теплот сгорания в зависимости от стадии метаморфизма при
этом имеет максимум, приходящийся на стадию потери большинства атомов
кислорода, после чего потеря атомов серы и водорода приводит к снижению этих
величин.
Таким образом, измеряя величины теплот сгорания
смолистых веществ нефти и сравнивая их с соответствующими величинами для смол,
элементарный состав, строение и генезис которых вполне ясны, можно решать
вопросы происхождения смол нефтей.
Следует, конечно, иметь в виду, что при таких тепловых
подсчетах мы получаем усредненные данные, характеризующие в целом всю сложную
смесь веществ, входящих в состав смол. Преобладание той или иной группы веществ
различного происхождения отразится на величинах теплот сгорания, но не даст еще
окончательных данных для однозначного решения вопроса. Окончательное решение
может быть найдено применением этого метода к исследованиям отдельных узких
фракций смол.
От величин теплот сгорания можно обычным путем перейти
к величинам свободной энергии смолистых веществ.
Имея в виду, что всякое органическое соединение,
содержащее в своем составе кислород, находится на более низком уровне свободной
энергии, чем соответствующий ему углеводород, а введение атомов серы вместо
атомов водорода несколько повышает уровень свободной энергии соединения, можно
считать, что отщепление в любой форме кислорода из состава сложной молекулы
повышает энергетический уровень остатка. В то же время отщепление атома серы
или азота может привести только лишь к небольшому изменению свободной энергии.
В целом при процессах изменения исходного органического вещества, содержащего
атомы кислорода, серы и азота, в зависимости от содержания водорода в системе
остающаяся часть более или менее повышается на шкале свободных энергий,
вероятно, все же оставаясь в пределах отрицательных значений. При достаточном
количестве водорода в системе известная часть углерода перейдет в состояние
связи с водородом, дав начало углеводородам.
Первичные смолистые вещества ввиду достаточного запаса
в них водорода могут дать начало некоторым количествам углеводородов. Смолы
окислительного происхождения, образовавшиеся главным образом из ароматических
углеводородов и первичных смол, не обладают достаточными количествами водорода
и не могут служить источниками новых количеств углеводородов. Следовательно,
различия между смолами окислительного происхождения и смолами первичными можно
видеть в первую очередь в различиях элементарного состава (относительно большее
содержание водорода в первичных смолах) и величины свободной энергии, большей
так же у первичных смол.
Теоретический анализ процессов, происходящих внутри системы
веществ нефти, приводит к выводу о генетически различных группах смолистых
веществ.
1.
Смолы
первичные, представляющие собой реликтовую форму вещества, отделившиеся в виде
раствора в углеводородах от материнской частицы.
2.
Смолы,
образовавшиеся в обстановке отсутствия окислителей из:
а) смол первичных,
б) углеводородов нефти.
3.
Смолы
окислительного происхождения, образовавшиеся из:
а) смол первичных,
б) углеводородов нефти,
в) смолистых продуктов преобразования первичных смол в
восстановительных условиях,
г) углеводородных смол.
Первые две группы смол вполне очевидно различаются по
элементарному составу, строению и некоторым другим свойствам. Более трудной
задачей является установление существенных различий в пределах третьей группы -
смол окислительного происхождения, но и эта задача не является совершенно
неразрешимой, так как каждая подгруппа смолистых веществ окислительного
происхождения имеет свои характерные признаки. Опираясь на эти последние с
обязательным учетом геохимической истории исследуемой системы нефти (битума) и
применяя современные методы разделения сложных смесей (возможно, дополненные
заново разработанными методами), можно будет составить более или менее
обоснованное заключение о процессах, приведших к образованию той или иной
сложной системы смолистых веществ.
В табл. 1 приводятся некоторые характерные признаки
отдельных групп смолистых веществ различного происхождения. Разумеется, что
приведенная таблица представляет собой лишь первую попытку разобраться в этих важных
показателях. По мере развития наших представлений о процессах образования
смолистых веществ, по мере разработки новых, более совершенных методов
исследования и накопления качественного фактического материала о деталях их
состава и строения предложенные здесь критерии, вероятно, подвергнутся
уточнению и дополнению. Особую роль при этом должны сыграть новые методы
разделения сложной смеси природных смолистых веществ на отдельные группы.
Из рассмотрения критериев генетического различия
отдельных групп смолистых веществ особенно наглядно вытекает
неудовлетворительность существующей классификации. В самом деле, деление
смолистых веществ на карбены и карбоиды, асфальтены и различные группы смол, в
том числе и на асфальтогеновые кислоты и их ангидриды, основано на случайных
физико-химических признаках и не отражает генетической сущности заключенных в
этих группах веществ. Например, к группе асфальтенов должны быть отнесены как
продукты превращения первичных смол, так и продукты далеко зашедшего
превращения углеводородов наряду с некоторыми группами смол окислительного
происхождения. Имеются основания считать, что в группу асфальтенов входят
высокомолекулярные продукты, состоящие целиком только из углерода и водорода, а
также и смолистые вещества, образовавшиеся из кислородных, сернистых и
азотистых соединений. В составе тех и других отсутствуют вещества с подвижными
атомами водорода. Кроме того, экспериментальные данные говорят о том, что
асфальтены могут возникнуть и в результате окислительных превращений силикагелевых
смол. Аналогичные соображения заставляют считать, что и группа собственно смол
не является однородной, а включает в себя представителей нескольких
генетических рядов.
Для смолистых веществ, выделенных из одной и той же
нефти, нет оснований предполагать обязательного наличия всех возможных групп
смолистых веществ, особенно смол окислительного происхождения. Это несколько yпpoщает задачу и делает более оптимистичным прогноз дальнейшего развития
экспериментальных методов изучения. смолистых веществ.
При составлении статьи существенную помощь своими
советами оказал нам М. Ф. Двали. Автор пользуется случаем выразить М.Ф. Двали
свою благодарность.
ЛИТЕРАТУРА
1. Андреев П.Ф.,
Иванцова В. В., Полякова Н.Н., Силина Н.П. Свойства и строение рассеянного органического вещества
осадочных пород. Геол. сб. 1. Тр. ВНИГРИ, вып. 83, 171. Гостоптехиздат, 1955.
2. Гуляева Л.А., Иткина Е.Е. Окислительно-восстановительный потенциал и
pH каустобиолитов. Тр. Ин-та нефти АН СССР, т. 3, 176, 1954.
3. Добрянский А.Ф.,
Андреев П. Ф.
Термодинамика процессов образования и изменения нефтей в природе. Изв. АН Эст.
ССР, т. 11. № 2, 1954.
4. Добрянский А.Ф. Термокаталитические превращения
углеводородов. ЖОХ, XXIII (XXXV), 1116, 1953.
5. Добрянский А. Ф. Геохимия нефти. Гостоптехиздат,
1948.
6. Коршак В.В. Химия высокомолекулярных
соединений. Изд. АН СССР, 1950.
7. Коттрел Т. Прочность химических связей. Изд. ин.
лит., 1956.
8. Морозова М. К вопросу о составе карбоидов. Тр.
ВНИГРИ, вып. 6, 130, 1954.
9. Revenda J.,
Szybinski V.
Аналитическая оценка кислых смол из нефти. Chem. Technik, V, 6, № 5, 284-287, 1954.
10. Сергиенко С.Р., Делоне
И.О. и др. Состав и свойства смолистой части дорийской нефти. Ст. 1. Тр. Ин-та
нефти АН СССР, т. 6, 1955.
11. Сергиенко С.Р. и др. Исследование состава и
свойств высокомолекулярной части нефти. Ст. 2. Тр. Ин-та нефти АН СССР, т. 6,
1955.
12. Семенов Н.Н. О некоторых проблемах химической
кинетики и реакционной способности. Изд. АН СССР, 1954.
13. Сыркин Я.И., Дяткина М.П. Химическая связь и строение молекул.
Госхимиздат. 1946.